Natria duuraniato
Natria duuraniato | |||||
 | |||||
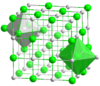
Kemia strukturo de natria duuraniato | |||||
 | |||||
Kristala strukturo de natria duuraniato | |||||
Alternativa(j) nomo(j) | |||||
| |||||
| Kemia formulo | Na2U2O7 | ||||
| CAS-numero-kodo | 13721-34-1 | ||||
| PubChem-kodo | 160982 | ||||
Fizikaj proprecoj | |||||
| Aspekto | Flava pulvoro | ||||
| Molmaso | 634.03 g mol−1 | ||||
| Denseco | 6.44 g/cm3 | ||||
| Fandopunkto | 1,646 °C | ||||
| Solvebleco | Akvo:Nesolvebla | ||||
Sekurecaj Indikoj | |||||
| Risko | R26/28 R33 | ||||
| Sekureco | S(1/2) S20/21 S45 | ||||
Pridanĝeraj indikoj | |||||
Danĝero
| |||||
GHS etikedigo de kemiaĵoj[1] | |||||
| GHS Damaĝo-piktogramo |
| ||||
| GHS Signalvorto | Damaĝa | ||||
| GHS Deklaroj pri damaĝoj | H300+330, H373, H411 | ||||
| GHS Deklaroj pri antaŭgardoj | P260, P264, P270, P271, P273, P284, P301+310, P304+340, P310, P320, P330, P391, P403+233, P405, P501 | ||||
Escepte kiam indikitaj, datumoj estas prezentataj laŭ iliaj normaj kondiĉoj pri temperaturo kaj premo (25 °C kaj 100 kPa) | |||||
Natria duuraniato, duuraniato de natrio aŭ Na2O (UO3)2 estas urania neorganika salo konata kiel flava oksido de uranio. Kune kun amonia duuraniato, ĝi estas unu el la komponaĵoj de la urania flava torto, iu miksaĵo da uraniaj oksidoj.
En la klasika metodo por ekstratado de uranio, la uraninito (aŭ UO2) estas rompita per miksaĵo da sulfata kaj nitrata acidoj. La uranio dissolviĝas por formado de "uranila sulfato", kaj natria hidroksido aldoniĝas por precipitigi la uranion kiel natria duuraniato. Ĉi-antikva metodo por uraniekstratado el ercoj de uraninito nuntempe estas anstataŭita procezoj tiel kiel persolvaĵa ekstratado, jona interŝanĝo kaj metodoj pri volatileco.
En la pasinteco ĝi estis grande uzita por produktado de urania vitro aŭ vazelina vitro, pro tio ke la natria salo facile dissolviĝas en silika matrico dum la ekbrulado de la komenca fando.
Enhavo
1 Sintezoj
1.1 Sintezo 1
1.2 Sintezo 2
1.3 Sintezo 3
2 Literaturo
3 Referencoj
Sintezoj |
Sintezo 1 |
- Fandoj de stekiometriaj kvantoj da natria karbonato kaj urania trioksido:
Na2CO3+2UO3 →800oC Na2U2O7+CO2↑{displaystyle {mathsf {Na_{2}CO_{3}+2;UO_{3} {xrightarrow {800^{o}C}} Na_{2}U_{2}O_{7}+CO_{2}uparrow }}} |
Sintezo 2 |
- Ekde natria uranila karbonato kaj natria hidroksido[2]:
2Na4UO2(CO3)3+6NaOH →800oC Na2U2O7+6Na2CO3+3H2O{displaystyle {mathsf {2;Na_{4}UO_{2}(CO_{3})_{3}+6;NaOH {xrightarrow {800^{o}C}} Na_{2}U_{2}O_{7}+6;Na_{2}CO_{3}+3;H_{2}O}}} |
Sintezo 3 |
- Ekde natria uranila karbonato kaj natria hidroksido[3]:
2UO2(CO3)34−+14NaOH → Na2U2O7+6Na2CO3+8OH−+3H2O{displaystyle {mathsf {2;UO_{2}(CO_{3})_{3}^{4-}+14;NaOH {xrightarrow {}} Na_{2}U_{2}O_{7}+6;Na_{2}CO_{3}+8;OH^{-}+3;H_{2}O}}} |
Literaturo |
- Chemical Book
- T3DB
Nanjing Chemlin Chemical Co. Ltd.- GuideChem
- Characterisation and Quality Control of Nuclear Fuels
Kent and Riegel's Handbook of Industrial Chemistry and Biotechnology, James A. Kent
Uranium Resource Processing: Secondary Resources, Chiranjib Gupta, Harvinderpal Singh
Uranium · Plutonium Transplutonic Elements, Harold C. Hodge, J.N. Stannard, J.B. Hursh
Nuclear Energy and the Environment: Environmental Sciences and Applications, Essam E. El-Hinnawi
Chemistry Of Lanthanides And Actinides, G. Singh- Advanced Inorganic Chemistry Vol-1
| ||||||
| ||||||
Referencoj |
↑ Ibilabs
↑ Advanced Inorganic Chemistry Vol-1
↑ Production of yellow cake and uranium fluorides